Definición de Aminas

Ingeniera Química
Las aminas son compuestos orgánicos considerados nitrogenados ya que derivan del compuesto amoníaco (NH3). En esta estructura química, uno o más grupos alquilo se unen al nitrógeno. Por ello, se forma un tetraedro distorsionado, ya que el nitrógeno estará unido a los grupos alquilo pero tendrá un par no enlazado de electrones libres.
Ejemplos de compuestos de aminas
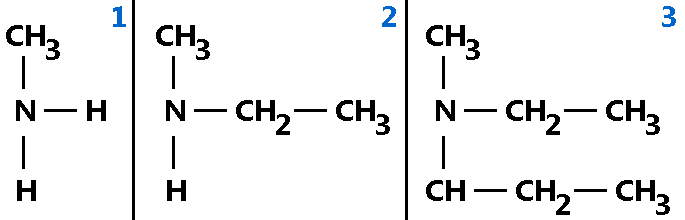
Como se puede observar en los gráficos, en función del tipo de grupo alquilo al que se une el nitrógeno será el nombre de la amina cuya nomenclatura sigue las reglas de los compuestos orgánicos. Por ejemplo, el caso uno cuyo nitrógeno está unido a un grupo metilo, designando el prefijo “metil”, por lo que, amina 1 es llamada a metil – amina. En el segundo caso, el nitrógeno se encuentra asociado a un grupo metilo y un grupo etilo, por lo que su nombre será metil – etil – amina. El tercer caso, hace referencia a una amina que contiene un grupo metilo y dos grupos etilo. De allí deriva su nombre: metil – dietil – amina. En todos los casos, se debe colocar el sufijo -amina.
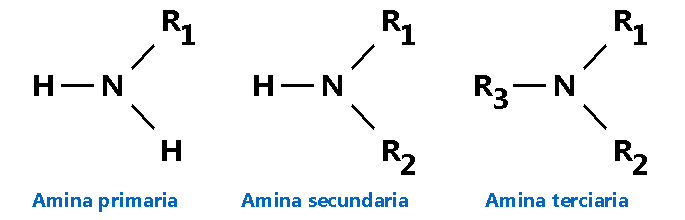
En función de la cantidad de grupos alquilo unidos al nitrógeno deriva el tipo de amina. Cuando se une a un único grupo alquilo, la amina se considera de tipo primaria. Cuando la amina contiene dos grupos alquilo, se denomina amina secundaria y, por último, si la amina contiene 3 grupos alquilo, se considera amina de tipo terciaria.
Obtención
Una vez que identificamos el tipo de compuesto, es muy simple comprender la reacción de formación de una amina, ya que deriva del amoníaco. Combinando este último con ioduros alcohólicos, por ejemplo, se obtienen las aminas y además HI. De allí la diferencia principal con el amoníaco, que las mismas son inflamables (mientras que el amoníaco no es lo en presencia de oxígeno) y esto se debe a que su estructura molecular posee átomos de carbono.
Otra forma de obtención es a través de un mecanismo conocido como Transposición de Hofmann, la cual convierte los compuestos de amidas en aminas con un carbono menos. También existen otras formas de obtención, como la síntesis de Gabriel o la reducción de azidas.
Dentro del mundo de la química orgánica, la obtención de aminas es un capítulo complejo y extenso, que trabaja con cada reacción de síntesis de manera muy particular.
Propiedades y aplicaciones
Las aminas son compuestos polares y también algunas de ellas cuentan con fuerzas de enlace Puente de Hidrógeno, lo cual infiere en altos puntos de ebullición. Por ejemplo, el caso de las aminas primarias y secundarias, contienen enlace puente de hidrógeno entre N – H. En el caso de la amina terciaria, esto no ocurre, sin embargo, podría suceder al unirse a moléculas con enlaces O – H. De allí, es que las aminas terciarias tienen puntos de ebullición menores que aminas primarias o secundarias cuyos pesos moleculares sean similares.
Su olor es característico, siendo el típico olor a pescado podrido o descompuesto, por ello, al trabajar con estos compuestos se debe cuidar la protección personal (utilización de guantes, gafas y máscaras adecuadas).
Las aminas, a su vez, forman parte de distintos compuestos biológicos y tienen funciones muy importantes, como ser biorreguladoras, actúan en mecanismos de defensa, entre otras. Dentro de los compuestos nitrogenados, se ubican las aminas biógenas, presentes en alimentos como la cerveza, el vino y los embutidos, ya que se obtienen a partir de la fermentación con bacterias. Dentro de las aminas biógenas más conocidas se encuentran la tiramina y la histamina, conocidas también por causar muchos problemas alimenticios e intoxicaciones y el principal alimento contenedor es el queso. Mucho se ha estudiado de ellas y se han encontrado distintas causas de su toxicidad, sin embargo, cabe destacar que la amina no es riesgosa por sí sola, sino por la reacción con otras sustancias, el consumo en conjunto con medicamentos y también la tolerancia propia de cada individuo.
Se las considera buenas neutralizadoras y con grandes capacidades emulsionantes y lubricantes.
Son consideradas bases débiles y capaces de neutralizar compuestos ácidos, manteniendo pH en rangos acotados. Por ello, es tan amplia su aplicación. Caso típico es el uso de soluciones de aminas en el endulzamiento de gas. Cuando el gas natural contiene CO2 y H2S, es tratado en plantas de procesamiento de aminas para la absorción de estos dos compuestos por la solución de amina. Posteriormente, el que era gas amargo se limpió, eliminado los contaminantes y la amina es enviada a otra torre de regeneración para revertir el ciclo, eliminado el CO2 y H2S absorbido y pudiendo ser enviada nuevamente a una torre contactora con el gas amargo para reiniciar un nuevo ciclo. Estas plantas de tratamiento con aminas se encuentran en Refinerías o Plantas de Fraccionamiento.
Las aplicaciones posibles son infinitas y dependerá de la utilización que se le quiera dar la forma en que se obtiene la amina, las propiedades y su tratamiento.

Trabajo publicado en: Ene., 2023.
Escriba un comentario
Contribuya con su comentario para sumar valor, corregir o debatir el tema.Privacidad: a) sus datos no se compartirán con nadie; b) su email no será publicado; c) para evitar malos usos, todos los mensajes son moderados.